
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
Dakle, dok se krećete niz grupu na periodnom sustavu, elektronegativnost elementa se smanjuje jer povećani broj energetskih razina stavlja vanjske elektrone vrlo daleko od privlačenja jezgre. Elektronegativnost povećava kako se krećete s lijeva na desno kroz razdoblje u periodnom sustavu.
Što se toga tiče, zašto se elektronegativnost smanjuje u skupini?
Elektronegativnost . Kretanje prema dolje u a skupina , the elektronegativnost se smanjuje zbog veće udaljenosti između jezgre i ljuske valentnog elektrona, čime se smanjuje privlačnost, zbog čega atom ima manju privlačnost za elektrone ili protone.
Nakon toga, postavlja se pitanje ima li elektronegativnost trend? Što je veća elektronegativnost atoma, veća je njegova sposobnost da privuče zajedničke elektrone. The elektronegativnost atoma raste kako se krećete s lijeva na desno kroz period u periodnom sustavu. The elektronegativnost atoma se smanjuje kako se krećete od vrha do dna niz grupu u periodnom sustavu.
Također se može zapitati kakav je trend pada energije ionizacije u skupini?
Krećući se slijeva nadesno kroz period, atomski radijus se smanjuje, pa se elektroni više privlače (bližoj) jezgri. Općenito trend je za energija ionizacije smanjiti kretanje odozgo prema dolje dolje periodni sustav skupina . Kretanje niz grupu , dodaje se valentna ljuska.
Kakav je trend padanja atomskog broja u grupu?
- The broj razina energije raste kako se krećete niz grupu kao broj elektrona raste. Svaka sljedeća razina energije je dalje od jezgre od posljednje. Stoga, atomski radijus raste kako se skupina a razina energije se povećava. 2) Dok se krećete kroz razdoblje, atomski radijus se smanjuje.
Preporučeni:
Kako pronalazite intervale povećanja i smanjenja?

Derivat funkcije može se koristiti za određivanje raste li funkcija ili opada u bilo kojem intervalu u svojoj domeni. Ako je f'(x) > 0 u svakoj točki u intervalu I, onda se kaže da funkcija raste na I. f'(x) < 0 u svakoj točki intervala I, tada se kaže da je funkcija opadajuća na I
Dolazi li do smanjenja kromosoma u mejozi?

Stanice koje prolaze kroz mejozu su diploidne. Redukcija kromosoma se događa u mejozi-1 kako bi se formirale 2 stanice koje su podvrgnute mejozi-2 kako bi se formirale četiri haploidne stanice (koji imaju polovicu broja kromosoma stanice koja prolazi kroz mejozu). Mejoza 2 je poput mitoze
Kako odrediti je li veza polarna bez tablice elektronegativnosti?

Korak 2: Identificirajte svaku vezu kao polarnu ili nepolarnu. (Ako je razlika u elektronegativnosti za atome u vezi veća od 0,4, vezu smatramo polarnom. Ako je razlika u elektronegativnosti manja od 0,4, veza je u biti nepolarna.) Ako nema polarnih veza, molekula je nepolarni
Koji je periodični trend za veličinu atoma od vrha do dna u skupini?

Od vrha do dna grupe, elektronegativnost se smanjuje. To je zato što se atomski broj povećava niz skupinu, a time postoji povećana udaljenost između valentnih elektrona i jezgre, odnosno veći atomski radijus
Tijekom koje diobe dolazi do smanjenja broja kromosoma u mejozi?
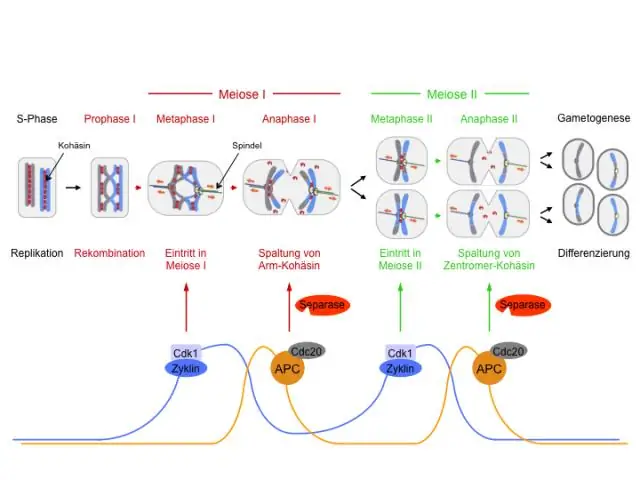
Prva podjela naziva se redukcijska podjela – ili mejoza I – jer smanjuje broj kromosoma sa 46 kromosoma ili 2n na 23 kromosoma ili n (n opisuje jedan kromosomski skup)
