Sadržaj:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
Molekularne formule reći vam koliko atoma svakog elementa ima u spoju, i empirijske formule reći vam najjednostavniji ili najsmanjeniji omjer elemenata u spoju. Ako je spoj molekularna formula ne može se više smanjiti, tada empirijska formula je isto što i molekularna formula.
Jednostavno, kako pronaći molekularnu formulu iz empirijske formule?
Molarnu masu spoja podijelite s empirijska formula masa. Rezultat bi trebao biti cijeli broj ili vrlo blizak cijelom broju. Pomnožite sve indekse u empirijska formula cijelim brojem pronađenim u koraku 2. Rezultat je molekularna formula.
koja je empirijska formula spoja čija je molekulska formula s6o9? ako je molekulska formula je S6O9 da biste dobili empirijska formula tražimo broj koji će podijeliti na 6 i 9 do pet najmanji omjer cijelih brojeva (što je definicija empirijska formula !).
Jednostavno, kako pronaći molekularnu formulu iz empirijske formule i molarne mase?
Empirijska formula težina = (1 x 12,01 g/mol) + (2 x 1,01 g/mol) + (1 x 16,00 g/mol) = 30,02 g/mol. Podijelite molekulska masa za molekularna formula od strane empirijska formula masa . Rezultat određuje koliko puta treba pomnožiti indekse u empirijska formula da biste dobili molekularna formula.
Kako rješavate empirijsku formulu?
Izračun empirijske formule
- Korak 1: Dobijte masu svakog prisutnog elementa u gramima. Element % = masa u g = m.
- Korak 2: Odredite broj molova svake vrste prisutnih atoma.
- Korak 3: Podijelite broj molova svakog elementa s najmanjim brojem molova.
- Korak 4: Pretvorite brojeve u cijele brojeve.
Preporučeni:
Zašto je empirijska formula magnezijeva oksida MgO?

Empirijska formula za magnezijev oksid je MgO. Magnezij je +2 kation, a oksid je -2 anion. Budući da su naboji jednaki i nasuprot ova dva iona će se povezati zajedno u omjeru atoma 1 prema 1
Koja je empirijska formula oktana?

C8H18 Ovdje, koja je empirijska formula oktana c8h18? The empirijska formula oktana $$C_{8}H_{18}$$ je: A. B. C. Slično tome, koja je empirijska formula c2h6o2? Molekularne i empirijske formule Pitanje Odgovor Napišite empirijsku formulu za sljedeći spoj:
Koja je empirijska formula za kofein?
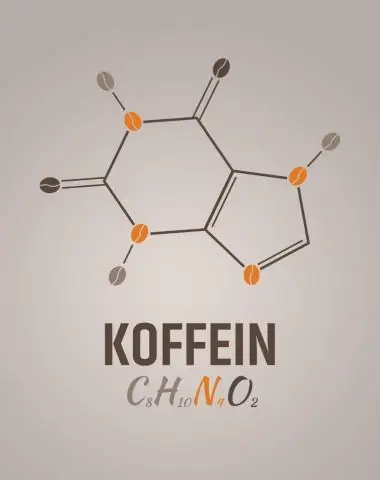
2 odgovora. C8H10N4O2 je molekularna formula za kofein
Koja je empirijska formula za stroncij bromid?

SrBr2 Onda, koja je formula za stroncij bromid? SrBr2 Osim toga, je li stroncij bromid voden? Oko Stroncijev bromid Heksahidrat Ultra visoke čistoće, visoke čistoće, submikroni i oblici nanopraška mogu se uzeti u obzir. Većina metala bromid spojevi su topljivi u vodi.
Koja je empirijska formula spoja?

Empirijska formula spoja je najjednostavniji omjer cijelih brojeva svake vrste atoma u spoju. Može biti ista kao i molekularna formula spoja, ali ne uvijek. Empirijska formula može se izračunati iz informacija o masi svakog elementa u spoju ili iz postotka sastava
