
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
Naći ograničavajući reagens gledajući broj molova svakog od njih reaktant . Odredite uravnoteženu kemikaliju jednadžba za kemijsku reakciju. Pretvorite sve dane informacije u molove (najvjerojatnije, korištenjem molarne mase kao faktora konverzije). Izračunajte molski omjer iz danih podataka.
Posljedično, koji je granični reaktant u jednadžbi?
Ograničavajući reaktant - The reaktant u kemijskoj reakciji koja ograničava količinu proizvoda koji se može formirati. Reakcija će prestati kada se sve ograničavajući reaktant se konzumira. Višak reaktanta - The reaktant u kemijskoj reakciji koja ostaje kada reakcija prestane kada se ograničavajući reaktant potpuno se potroši.
Slično tome, koji je ograničavajući reaktant u vodi? Kisik (O2) proizvodi manje voda (H2O) nego vodik (H2) dakle kisik je ograničavajući reaktant.
Ovdje se objašnjava što je ograničavajući reagens?
The ograničavajući reagens (ili ograničavajući reaktant ili ograničavajući agens) u kemijskoj reakciji je tvar koja se potpuno potroši kada je kemijska reakcija gotova. Količina nastalog proizvoda ograničena je ovim reagens , budući da se reakcija ne može nastaviti bez toga.
Kako pronaći molove produkta ograničavajućeg reaktanta?
Ako vam se da madeži sadašnjost svake reaktant , i zamolio pronaći the ograničavajući reaktant određene reakcije, tada najjednostavniji način da pronaći koji je ograničavajući je podijeliti svaku vrijednost s odgovarajućim koeficijentom te tvari u (uravnoteženoj) kemijskoj jednadžbi; koja god vrijednost je najmanja je ograničavajući reaktant.
Preporučeni:
Što znači ograničavajući faktor ovisan o gustoći?
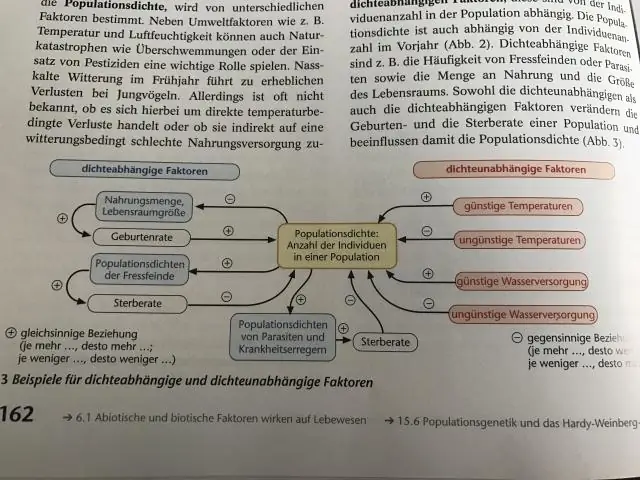
Ograničavajući čimbenici ovisni o gustoći Faktori ovisni o gustoći su čimbenici čiji učinci na veličinu ili rast populacije variraju s gustoćom naseljenosti. Postoje mnoge vrste ograničavajućih čimbenika ovisnih o gustoći kao što su; dostupnost hrane, grabež, bolesti i migracije
Zašto je Daltonov zakon ograničavajući zakon?

Ograničenje Daltonovog zakona Zakon vrijedi za stvarne plinove pri niskom tlaku, ali pri visokom tlaku značajno odstupa. Smjesa plinova je nereaktivne prirode. Također se pretpostavlja da je interakcija između molekula svakog pojedinog plina ista kao i molekula u smjesi
Što znači ograničavajući faktor?

Definicija ograničavajućeg faktora. 1: faktor koji ograničava brzinu reakcije u bilo kojem fiziološkom procesu kojim upravljaju mnoge varijable. 2: okolišni čimbenik koji je od prevladavajuće važnosti u ograničavanju veličine populacije nedostatak zimskog pregleda je ograničavajući čimbenik za mnoga stada jelena
Je li hrana ograničavajući faktor?

Neki primjeri ograničavajućih čimbenika su biotički, poput hrane, partnera i natjecanja s drugim organizmima za resurse. Na primjer, ako u šumi nema dovoljno plijena za prehranu velike populacije grabežljivaca, tada hrana postaje ograničavajući čimbenik
Zašto je intenzitet svjetlosti ograničavajući čimbenik fotosinteze?

Intenzitet svjetla Bez dovoljno svjetla, biljka ne može vrlo brzo fotosintetizirati - čak i ako ima puno vode i ugljičnog dioksida te prikladnu temperaturu. Povećanje intenziteta svjetlosti povećava brzinu fotosinteze, sve dok neki drugi čimbenik – ograničavajući faktor – ne postane manjak
