
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
U vodikovom spektru, neki spektralne linije su svjetlije od ostalih ovisno o njihovoj energetskoj razini. Kada elektron skoči s neke više orbite, energija se oslobađa u fotonu htjeti biti veći i dobivamo a svjetlije crta. Tako u vodikovom spektru neki linije su svjetlije nego drugi.
Također treba znati koji element ima najviše spektralnih linija?
Merkur: najjači crta , na 546 nm, daje živi zelenkastu boju. Slika 2. Kada se zagrije u cijevi za električni pražnjenje, svaki element stvara jedinstveni uzorak spektralni ` linije '.
Može se također pitati, što je širenje spektralnih linija? Proširenje linije . spektroskopija. Proširenje linije , u spektroskopiji, širenje preko veće valne duljine ili frekvencijskog raspona apsorpcije linije (tamno) ili emisija linije (svijetlo) u zračenju primljenom od nekog objekta.
Na ovaj način, zašto su spektralne linije različite za svaki element?
Svaki element emisija spektar razlikuje se jer svaki element ima različit skup energetskih razina elektrona. The linije (fotoni) se emitiraju kako elektroni padaju s orbitala više energije na niže energije.
Kako prepoznati spektralnu liniju?
Emisija linije se vide kao obojene linije na crnoj pozadini. Apsorpcija linije se vide kao crne linije na obojenoj pozadini. Prisutnost spektralne linije objašnjava kvantna mehanika u smislu energetskih razina atoma, iona i molekula.
Preporučeni:
Može li hi kvadrat biti negativan?
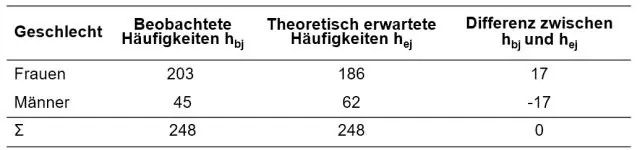
Mislite li: mogu li vrijednosti hi kvadrata ikada biti negativne? Odgovor je ne. Vrijednost chi kvadrata ne može biti negativna jer se temelji na zbroju kvadrata razlika (između dobivenih i očekivanih rezultata)
Koliko dugo nakon potresa može biti naknadnih potresa?

Deset dana nakon glavnog potresa postoji samo desetina broja naknadnih potresa. Potres će se nazivati naknadnim potresom sve dok je stopa potresa veća nego što je bila prije glavnog potresa. Za velike potrese to bi moglo trajati desetljećima. Veći potresi imaju više i veće naknadne potrese
Može li biti vulkan u Los Angelesu?

U Los Angelesu nema vulkana. Najbliža vulkanska aktivnost je vulkansko polje Lavic i vulkansko polje Coso
Kako fitoplankton može biti štetan?

Kada je dostupno previše hranjivih tvari, fitoplankton može izrasti izvan kontrole i stvoriti štetno cvjetanje algi (HAB). Ovi cvjetovi mogu proizvesti iznimno otrovne spojeve koji imaju štetne učinke na ribe, školjke, sisavce, ptice, pa čak i ljude
Kako test pruga može biti od pomoći u identifikaciji minerala?

'Test strica' je metoda koja se koristi za određivanje boje minerala u prahu. Ispitivanje prugama radi se struganjem uzorka minerala preko komada neglaziranog porculana poznatog kao "ploča s prugama". To može proizvesti malu količinu minerala u prahu na površini ploče
