
Sadržaj:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
Koraci
- Pronađite atomski broj svog atoma.
- Odredi naboj atoma.
- Zapamtite osnovni popis orbitala.
- Razumjeti notaciju konfiguracije elektrona.
- Zapamtite redoslijed orbitala.
- Popunite orbitale prema broju elektrona u vašem atomu.
- Koristite periodni sustav kao vizualni prečac.
Slično tome, koji su koraci za pisanje konfiguracije elektrona?
Koraci
- Pronađite atomski broj svog atoma.
- Odredi naboj atoma.
- Zapamtite osnovni popis orbitala.
- Razumjeti notaciju konfiguracije elektrona.
- Zapamtite redoslijed orbitala.
- Popunite orbitale prema broju elektrona u vašem atomu.
- Koristite periodni sustav kao vizualni prečac.
Drugo, što je Subshell? A podljuska je podjela elektronskih ljuski odvojenih elektronskim orbitalama. Podljuske označeni su s, p, d i f u elektronskoj konfiguraciji.
Slično, postavlja se pitanje, što je Hund pravilo?
Hundovo pravilo . Hundovo pravilo : svaka orbitala u podljusci je pojedinačno zauzeta jednim elektronom prije nego što je bilo koja orbitala dvostruko zauzeta, a svi elektroni u jednostruko zauzetim orbitalama imaju isti spin.
Koliko je elektrona u svakoj ljusci?
Svaka ljuska može sadržavati samo fiksni broj elektrona: Prva ljuska može izdržati do dva elektrona , druga ljuska može zadržati do osam (2 + 6) elektrona, treća ljuska može zadržati do 18 (2 + 6 + 10) i tako dalje. Opća formula je da n-ta ljuska u principu može držati do 2(n2) elektroni.
Preporučeni:
Kako napisati konfiguraciju elektrona za MN?

Mangan, s druge strane, ima konfiguraciju elektrona od 1s22s22p63s23p64s23d5 i konfiguraciju plemenitog plina od [Ar]4s23d5, što rezultira jednim nesparenim elektronom u svakoj 3d sub-orbitali
Kako pronalazite konfiguraciju elektrona za kisik?

Prilikom pisanja elektronske konfiguracije za kisik prva dva elektrona ići će u 1s orbitalu. Budući da 1s može zadržati samo dva elektrona, sljedeća 2 elektrona za O idu u orbitalu 2s. Preostala četiri elektrona ići će u 2p orbitu. Stoga će konfiguracija O elektrona biti 1s22s22p4
Kako nacrtati jednadžbu korak po korak?
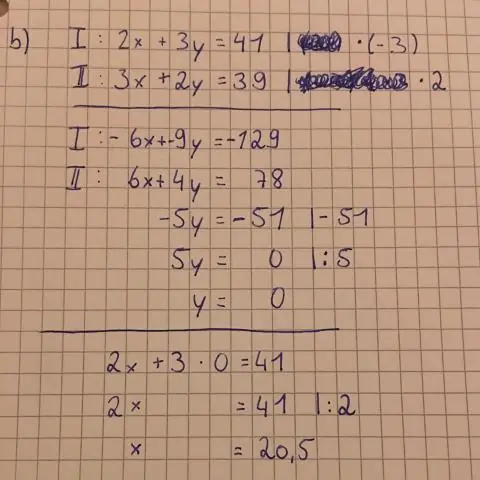
Evo nekoliko koraka koje treba slijediti: Uključite x = 0 u jednadžbu i riješite za y. Nacrtajte točku (0,y) na y-osi. Utaknite y = 0 u jednadžbu i riješite za x. Nacrtajte točku (x,0) na osi x. Nacrtajte ravnu liniju između dvije točke
Kako pronalazite konfiguraciju elektrona za srebro?

Konfiguracija elektrona osnovnog stanja plinovitog neutralnog srebra u osnovnom stanju je [Kr]. 4d10. 5s1, a simbol pojma je 2S1/2
Kako napraviti nagib korak po korak?

Postoje tri koraka u izračunavanju nagiba ravne linije kada vam nije dana njezina jednadžba. Prvi korak: Identificirajte dvije točke na liniji. Drugi korak: Odaberite jedan da bude (x1, y1), a drugi da bude (x2, y2). Treći korak: Koristite jednadžbu nagiba za izračunavanje nagiba
