
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
Dakle, mi izračunati to uzimanjem ponderiranog masa svakog od izotopa i zbrajajući ih. Dakle, za prvo masa , pomnožit ćemo 0,50% od 84 (amu - atomska masa jedinica) = 0,042 amu, i dodajte ga na 9,9% od 86 amu = 8,51 amu, i tako dalje.
Nakon toga, može se također pitati, kako izračunati prosječnu atomsku masu?
Izračunavanje prosječne atomske mase The prosječna atomska masa elementa je zbroj mise njegovih izotopa, svaki pomnožen sa svojim prirodnim obiljem (decimala povezana s postotkom atoma tog elementa koji su od danog izotopa). Prosječna atomska masa = f1M1 + f2M2 +…
Također znajte koje su tri vrste informacija potrebne za izračunavanje prosječne atomske mase? Broj izotopa koji postoje za element. The atomski Broj za element. Postotak obilja svakog izotopa.
Također se može zapitati koja je vrijednost najbliža atomskoj masi stroncija?
Stroncij . U svom izvješću iz 1961. Komisija je preporučila Ar(Sr) = 87,62 na temelju masa -spektrometrijsko određivanje Niera. Ovaj vrijednost revidiran je u Ar(Sr) = 87,62(1) 1969. godine i od tada ostaje nepromijenjena.
Što ima masu od 1 amu?
Jedinica atomske mase (simbolizirana AMU ili amu) definirana je kao točno 1/12 mase atoma ugljika-12. Atom ugljika-12 (C-12) ima šest protona i šest neutroni u svojoj jezgri. Neprecizno rečeno, jedan AMU je prosjek proton masa odmora i neutron masa mirovanja.
Preporučeni:
Kako pronaći prosječnu brzinu s dvije brzine?
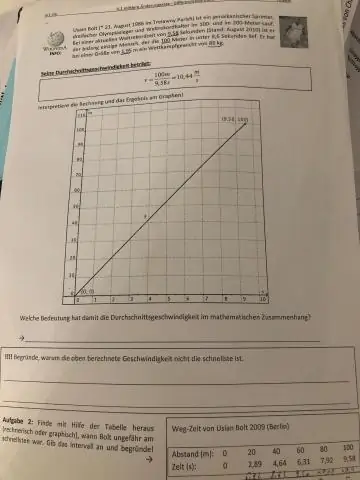
Zbroj početne i konačne brzine dijeli se s 2 da bi se dobio prosjek. Kalkulator prosječne brzine koristi formulu koja pokazuje da je prosječna brzina (v) jednaka zbroju konačne brzine (v) i početne brzine (u), podijeljen s 2
Imaju li svi atomi magnezija istu atomsku masu?

O: Magnezij, u svom elementarnom obliku, ima 12 protona i 12 elektrona. Neutroni su druga stvar. Prosječna atomska masa magnezija je 24,305 jedinica atomske mase, ali nijedan atom magnezija nema točno ovu masu
Kako izračunati atomsku masu bora?
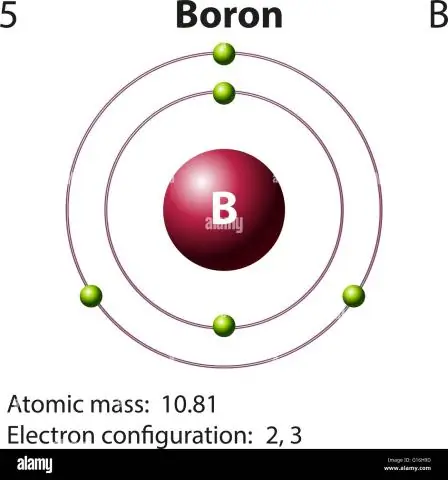
Za bor će ova jednadžba izgledati ovako: 5 protona + 5 neutrona = 10 jedinica atomske mase (AMU) ili, za češći izotop bora (približno 5 protona + 6 neutrona = 11 AMU
Koji element ima najveću atomsku masu?

Ununoctium je najteži element, ali ga je napravio čovjek. Najteži prirodni element je uran (atomski broj 92, atomska težina 238,0289)
Kako pronaći prosječnu brzinu na grafikonu brzine u odnosu na vrijeme?

Područje ispod krivulje brzina/vrijeme je ukupni pomak. Ako to podijelite s promjenom vremena, dobit ćete prosječnu brzinu. Brzina je vektorski oblik brzine. Ako je brzina uvijek nenegativna, tada su prosječna brzina i prosječna brzina iste
