
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Zadnja promjena 2025-01-22 16:59.
Drugi Ionizacija Energije uvijek su viši nego prvi zbog dva glavna razloga: uklanjate elektron s položaja koji je malo bliže jezgri, pa je stoga podložan veći privlačnost za jezgru.
Štoviše, zašto je druga energija ionizacije elementa uvijek veća od prve?
The druga energija ionizacije od Mg je veći od prvog jer to stalno uzima više energije ukloniti elektron s pozitivno nabijenog iona od od neutralnog atom.
zašto je prva energija ionizacije berilija veća od litija? Berilijum (Skupina II) ima dodatni elektron i proton u usporedbi s litij . Dodatni elektron ide u istu orbitalu 2s. Povećanje u energija ionizacije (I. E.) Slično, I. E. kisika je manje od onaj dušika jer je dodatni elektron zaštićen napola ispunjenom 2p orbitalom.
Drugo, zašto Li ima veću drugu energiju ionizacije od biti?
To je zbog povećanja nuklearnog naboja zbog dodavanja elektrona. Sada tvori Be+ koji je nestabilan, tako da dobiti stabilan (Be++). drugi elektron treba ukloniti, tako da smo potreba manje energije ukloniti taj elektron i stoga je druga ionizacija je više od toga Li.
Je li prva energija ionizacije veća od druge?
The energije uklanjanje jednog elektrona iz neutralnog atoma naziva se prva energija ionizacije , i energije potrebno ukloniti drugi elektron se naziva druga energija ionizacije . The druga energija ionizacije je, općenito, veći od the prva energija ionizacije.
Preporučeni:
Kako se zove kemikalija u kojoj se pohranjuje energija tijekom prve faze fotosinteze?
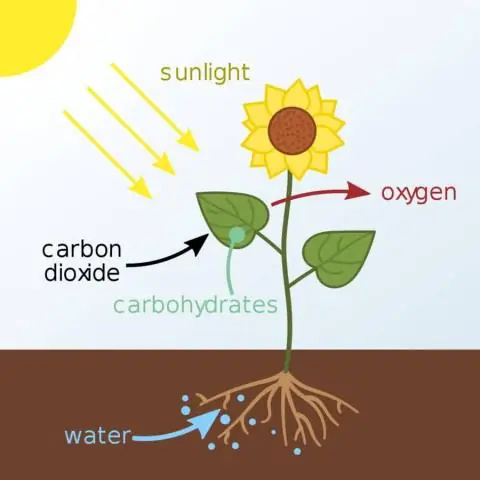
Reakcije ovisne o svjetlosti koriste svjetlosnu energiju za stvaranje dvije molekule potrebne za sljedeću fazu fotosinteze: molekulu za pohranu energije ATP i reducirani prijenosnik elektrona NADPH. U biljkama se svjetlosne reakcije odvijaju u tilakoidnim membranama organela zvanih kloroplasti
Zašto se povećava energija ionizacije?

Energija ionizacije elemenata raste kako se pomičemo gore u određenoj skupini jer se elektroni drže u orbitalama niže energije, bliže jezgri i stoga čvršće vezani (teže ih je ukloniti)
Pri usporedbi dviju populacija Što je veća standardna devijacija to je veća disperzija?

Kada se uspoređuju dvije populacije, što je veća standardna devijacija, to je veća disperzija distribucije, pod uvjetom da varijabla od interesa od dvije populacije ima isti skup mjera
Kolika je energija ionizacije kJ mol dušika?

Energija ionizacije molekularnog dušika je 1503 kJ mol?-1, a atomskog dušika 1402 kJ mol?-1. Još jednom, energija elektrona u molekularnom dušiku niža je od energije elektrona u odvojenim atomima, pa je molekula vezana
Zašto je neobično da grafit provodi struju?

Grafit kao mineral ugljika/ruda prirodno pokazuje električnu vodljivost. Može provoditi struju zbog velike količine slobodnih neograničenih elektrona koji lebde unutar njegovih ugljikovih slojeva. Ovi valentni elektroni mogu se slobodno kretati, pa su u stanju provoditi elektricitet
